过氧化氢(H2O2)超快检测试剂盒(200次)
发布时间:2023-11-08 分享至:
一. 产品简介
过氧化氢(H2O2)超快检测试剂盒利用H2O2与显色底物之间的反应,生成红色氧化产物,通过比色法或荧光法检测样品中的H2O2,反应在10 s内即可完成,检测限为0.02 μM,可实现H2O2的超快灵敏检测。
二. 试剂盒组成与存储
本试剂盒采用4 ⁰C运输,收货后请储存在-20 ⁰C。
试剂盒组成 | 数量 | 储存条件 | 保质期 |
显色液 | 100 μL | -20℃ | 12个月 |
增敏剂 | 1 mg | ||
缓冲液 | 25 mL | ||
H2O2母液 (10 mM) | 1 mL |
三. 实验步骤
1. 溶液配制
Ø 增敏剂溶液:将1 mg增敏剂溶解在1 mL缓冲液中,得到增敏剂溶液。
(注:增敏剂溶解后请按每管50 μL或100 μL分装保存至-20℃,避免反复冻融)
Ø 50 μM H2O2标准液:取10 μL H2O2母液(10 mM),加入至1.99 mL缓冲液并混匀,该标准液可在4 ℃长期储存。
Ø 检测液(以配制1 mL为例):取1 mL缓冲液,加入10 μL 显色液和50 μL 增敏剂溶液。(注:1 mL检测液可检测20次,但标准曲线绘制需消耗6次,请合理计算检测液配制量。检测液配制后,可在4℃避光保存24h,使用时避免强光照射)。
2. 分别取0、2.5、5、10、20、40 μL的50 μM H2O2标准液加入至96孔板中,并加入缓冲液补足至50 μL,得到浓度依次为0、2.5、5、10、20、40 μM的H2O2溶液。取50 μL待测样品溶液,加入至另外的空白孔中。
3. 向每个孔分别加入50 μL检测液,避光反应至少10s,通过酶标仪测定570 nm处吸光度,建立标准曲线,根据标准曲线计算样品溶液中H2O2浓度。
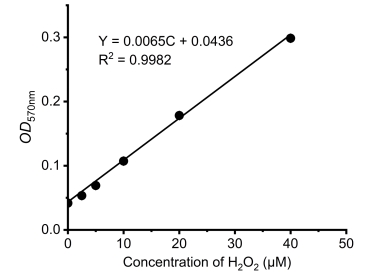
图1. 比色法建立的H2O2标准曲线
(受仪器和操作影响,本曲线仅供参考)
四. 注意事项
Ø 显色液对光敏感,请注意避光保存和使用,使用过程中避免长时间强光照射;
Ø 检测液须现配现用,若略微变红,仍可正常使用;若颜色明显变红,建议重配;
Ø 若检测过程中发现检测溶液先快速变红,后又褪色,说明待测样品溶液中H2O2浓度过高,使得显色底物氧化漂白。当待测样品溶液中H2O2浓度已经超过检测范围时,应将样品溶液稀释后再进行测定。
Ø 若检测溶液中存在H2O2之外的其他强氧化物质时,可能会导致假阳性。因此,建议增加不含H2O2的样品溶液作为对照。
Ø 向样品溶液中加入检测液10s内,溶液发生明显的显色反应,10s后即可检测出样品中的H2O2。随时间延长,显色底物会被水中的溶解氧缓慢氧化,长时间放置(约12小时),溶液颜色也会缓慢加深。因此,向样品溶液中加入检测液后应及时检测。
Ø 当样品溶液中H2O2浓度极低时,本试剂盒还可以通过荧光法检测H2O2,***低可检测0.02 μM的H2O2。具体步骤如下:
1)取5 μL的50 μM H2O2标准液,加入495 μL缓冲液,配制成0.5 μM H2O2标准液。
2)分别取0、2.5、5、10、20、40 μL的0.5 μM H2O2标准液加入至96孔板中,并加入缓冲液补足至50 μL,配制浓度分别为0、0.025、0.05、0.1、0.2、0.4 μM的H2O2标准溶液。取50 μL待测样品溶液,加入至另外的空白孔中。
3)向每个孔分别加入50 μL检测液,避光反应至少10s,采用酶标仪测定激发波长为540 nm,发射波长为590 nm处的荧光值,建立标准曲线,根据标准曲线计算样品溶液中H2O2浓度。
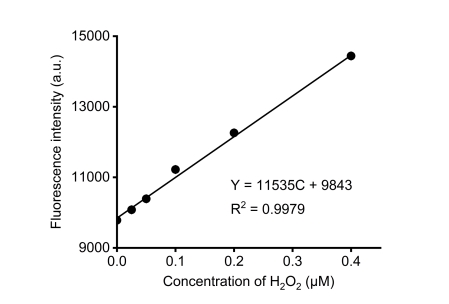
图2. 荧光法建立的H2O2标准曲线 (供参考)